- Introduction
- La lumière
- Cohérences et interférences
- Le laser
- Utilisation et dangers du laser
- Conclusion
La lumière
1. Lumière - Onde électromagnétique
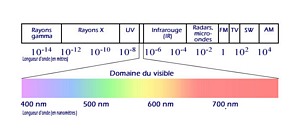
La lumière est un phénomène ondulatoire (qui subit des phénomènes de réflexion, de diffraction, de réfraction), elle fait partie d’un ensemble d’ondes appelées ondes électromagnétiques. Parmi ces ondes se trouvent différentes longueurs d’ondes : avant l’ultraviolet, elles sont inférieures à 400 nm et au-delà de l’infrarouge, elles sont supérieures à 800 nm. Elles représentent le domaine de la lumière invisible. Le reste correspond à la lumière visible et la lumière dite « blanche » comprend donc toutes ces ondes ; elle est polychromatique.
2. Lumière - Particule
Au sein même de l’atome, il existe des couches électroniques où gravitent les électrons. Chaque répartition des électrons sur les couches électroniques correspond à un niveau d’énergie de l’atome. La première couche, celle où les électrons ne possèdent aucune énergie, se nomme la couche fondamentale. Les autres couches sont en revanche l’endroit où s’est produit un gain d’énergie par les atomes : plus ceux-ci sont éloignés du noyau, et donc situés sur les couches électroniques supérieures, plus ceux-ci ont acquis de l’énergie. Pour produire de la lumière, il faut donc que les électrons aient acquis de l’énergie en se trouvant sur ces couches.
Pour qu’un atome acquière de l’énergie, il faut qu’un corps puisse exciter ses électrons. Ce corps c’est le photon. Il possède une masse nulle, est caractérisé par une fréquence et est doté d’énergie. Cette énergie peut être mesurée par les formules suivantes :
∆E = h · ν
∆E : l'énergie en Joules (J) ;
h : 6.63 · 10-34 J · s-1 ;
ν : la fréquence en Hertz (Hz)
L'atome peut subir plusieurs phénomènes quand un électron monte ou descend sur une couche électronique de l’atome. Lorsqu’il va monter, il va se produire une absorption ; quand il va descendre, une émission.
A. Absorption
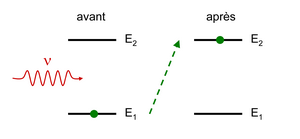
Quand le photon traverse l’atome, celui-ci va alors absorber cette énergie en la transférant à l’électron se situant sur sa couche fondamentale. Ce dernier va alors être dans un état excité et se placer à la couche électronique supérieure. Ceci ne peut s’opérer que si l’énergie perçue correspond exactement au passage de l’électron d’une couche à une autre. On dit que les couches électroniques sont quantifiées et cette quantité est appelé le quanta. C’est le principe de l’absorption.
B. Émission
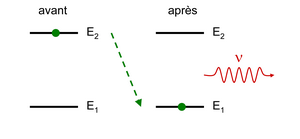
Mais quand un atome possède de l’énergie, il a tendance à toujours vouloir s’en débarrasser. Pour se faire, les électrons qui étaient sur les couches excités vont redescendre sur la couche fondamentale. Cette transition électronique, également quantifiée, va provoquer la libération d’un photon, d’énergie égale à l’énergie libérée par l’atome. Ce photon libéré se traduit par une émission de lumière, à une longueur d’onde précise, à une couleur précise. C’est ce qu’on appelle une émission spontanée d’un photon. Quand la libération de l’énergie s’opère sous forme lumineuse, on parle d’émissions de radiations.
C. Le train d’onde
Un photon n’est en fait qu’une simple onde électromagnétique qui possède une énergie. En vérité, dans un cas d’absorption comme d’émission, au niveau ondulatoire, c’est un paquet d’ondes qui est émis ou absorbé dans un temps donné ; ce paquet est un train d’ondes libéré ou émis pendant le temps de cohérence. Cette durée est très courte, environ 10-11 secondes (notée τc sur la figure). Il a aussi une étendue spatiale et temporelle finie car la source qui l'engendre à un début et une fin et sa propagation est limitée à un espace donné.
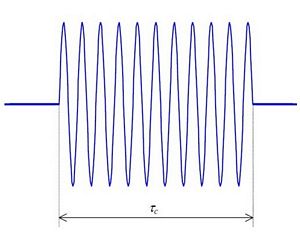
Sur la figure 3, ν ne correspond pas simplement à la libération d’un photon, c’est aussi la durée durant laquelle un train d’ondes vient de passer.
D. Saut quantique
Ce qui est surprenant lors de l’émission ou de l’absorption d’un photon, c’est que l’électron passe d’une orbite à une autre sans traverser l’espace qui les sépare. C’est comme si l’électron était « téléporté » d’une couche électronique à une autre en émettant un photon à une certaine longueur d’onde. En effet, on aurait pu croire que l’électron doit obligatoirement traverser l’espace se trouvant entre deux couches électroniques… Non, car autrement le photon émis n’aurait pas une couleur unique, une couleur franche, mais plutôt un dégradé.